近年、バイオテクノロジー技術を利用したペプチド、核酸やタンパクなどのバイオ医薬品の開発が加速しています。抗体医薬や活性部位を中心に設計されたペプチド医薬品やバイオシミラー(バイオ後続品)の開発が活発で、特性解析では種々の分析を駆使して構造を決定することが求められます。
特性解析
バイオ医薬品の特性解析(物理的化学的性質、生物活性、免疫化学的性質、純度及び不純物に関する解析など)は、適切な規格及び試験方法を設定するために重要です。
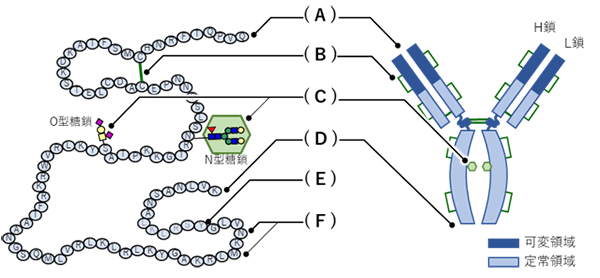
(A)N末端の修飾 (ピログルタミル化など)
(B)ジスルフィド結合の架け替え
(C)糖鎖の有無、種類の違い
(D)C末端アミノ酸残基の欠損
(E)断片化
(F)脱アミド化/酸化(Asnの脱アミド化、Metの酸化など)
安定性試験及び品質・規格試験
バイオ医薬品の品質を確保する上で、品質・規格試験は重要な規制基準です。
安定性試験は、医薬品の保存方法や有効期間を決定するための重要な試験です。
技術資料
- GMP体制下のSEC-MALS分析 凝集体の分子量評価
- キャピラリー電気泳動によるバイオ医薬品の品質評
- GMP規制下でのセルベースアッセイ
- SPRを用いたHost Cell Proteinの高感度検出法の構築
バイオ医薬品の生体試料中濃度測定
バリデートされた分析法を用いて、安全性試験や臨床試験で採取された血液(血漿や血清)中のバイオ医薬品の濃度を正確に定量します。
技術資料
免疫原性 (Immunogenicity)の評価
バイオ医薬品を動物やヒトに投与すると、それが異物と認識されて免疫反応が生じ、抗体(抗薬物抗体)が産生されることがあります。抗体が中和活性を持ったり、薬物動態を変化させ有効性や安全性に影響を及ぼす可能性があることから、抗体を測定することが重要です。
技術資料
分析メニュー
| メニュー | 項 目 | 詳 細 |
|---|---|---|
| 特性解析 | アミノ酸分析 | アミノ酸組成分析、DL-アミノ酸分析、アミノ酸分析計、HPLCにより測定 |
| 末端アミノ酸配列解析 | N末端(ブロックN末端)、アミノ酸配列解析、C末端アミノ酸配列解析、プロテインシーケンサー、MS/MS等により解析 | |
| ペプチドマップの作成 | 酵素消化後、HPLC又はLC-IT-TOF/MSにより作成 | |
| 全アミノ酸配列分析 | 酵素消化後のペプチドをLC/MS/MSにより解析、必要に応じてペプチドを分取後、プロテインシーケンサーにより解析 | |
| ジスルフィド結合位置の解析 | 還元及び非還元条件下で酵素消化後、LC/MS/MSにより解析、必要に応じてペプチドを分取後、プロテインシーケンサーにより解析 | |
| 抗体薬物複合体(ADC)の薬物抗体比及び結合位置の解析 | LC/MS、酵素消化後のペプチドをLC/MS/MSにより解析 | |
| 糖組成分析 | 中性糖、アミノ糖、シアル酸等のHPLCによる測定 | |
| 糖鎖構造解析 | PA化又はAB化等の蛍光標識糖鎖の糖鎖マップ法、LC/MS/MS、酵素消化法等による解析 | |
| 糖鎖結合位置の解析 | MS/MS及びプロテインシーケンサー等により解析 | |
| 分子量測定 | LC/MS、MALDI-TOF/MS、SDS-PAGE、ゲルろ過、凝集体分析 | |
| 電気泳動パターン | SDS-PAGE、等電点電気泳動(cIEF)、画像解析 | |
| 二次構造解析 | CD、NMRによる測定、解析 | |
| 生物活性 | 培養細胞を用いるバイオアッセイ、生化学的試験 | |
| 免疫化学的性質 | 結合試験(アフィニティー、交差反応性)、エピトープマッピング、標的分子の同定(イムノアッセイ、ウエスタンブロティング) | |
| 薬物動態 | 薬物濃度測定 | ELISA、ECL |
| 免疫原性 | ELISA、ECL |
医薬品の生産技術開発や、生産規模のスケールアップ、改良などによる変更前後の同等性/同質性評価(特性解析、安定性試験含む)の為に上記分析項目を用いて実施いたします。